成功案例
苯磺酸氨氯地平片一致性点评进展剖析
时间: 2024-02-12 03:05:59 | 作者: 华为网盘网页版登录入口
归于国家管控风险化学品,依据相关法规和网安部分规矩,本网站不供给该产品相关出售信息。
7月中旬,业界撒播出国家医保局关于药品4+7集采扩面企业座谈会纪要,其内容首要包含:
3. 企业规模:一切此轮开标前经过一致性点评种类的原研及仿制药出产企业;
4. 约好用量:悉数区域公立医院、定点民营医院、戎行医院上报用量按特别的份额作为约好量。若一家中标给予50%量,两家中标给60%量,三家中标给70%量;
5. 竞标规矩:一切企业(包含原研企业)以不高于4+7中标价格申报,报价的企业直接中选,其他企业顺次决议是不是承受报价,直到中选企业满 3 家(或3家以上,待决议计划)。依据报价凹凸,企业替换轮番选择省份(1,2,3,1,2,3),所选择省份报的量总和便是此企业约好的量;
6. 周期:2 家中标种类 1 年,3 家(或 3 家以上)中标种类 2-3 年;
另据了解,正式文件将于本年 10 月前宣告,年末投标,下一年开端履行。据此,业界也掀起了新一轮的药品降价潮。
那么,此前中选的25个通用名,其间标企业将面对哪些原研厂商及经过一致性点评厂家的应战?竞赛态势怎么?此外,到现在仿制药一致性点评申报状况怎么?7月份新经过的种类都有哪些?咱们带你先睹为快!
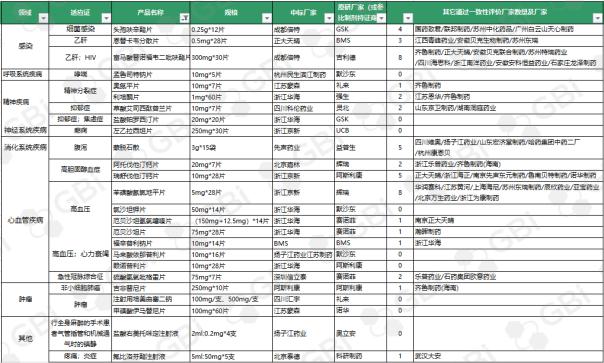
以上表格计算了到2019年7月29日,25个第一批4+7中标药品经过一致性点评的企业状况。
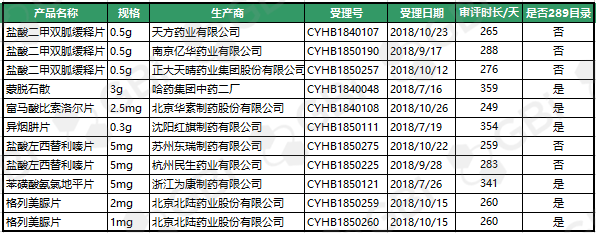
到2019年7月29日,7月份新增11个品规经过仿制药一致性点评。其间:6个品规为289目录种类。
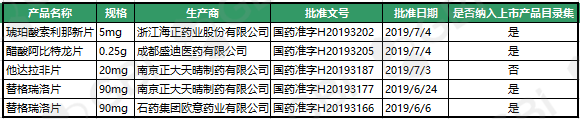
GBI SOURCE数据库显现,到2019年7月29日,7月份新增视同经过仿制药一致性点评品规5个,其间4个已被归入《我国上市药品目录集》。
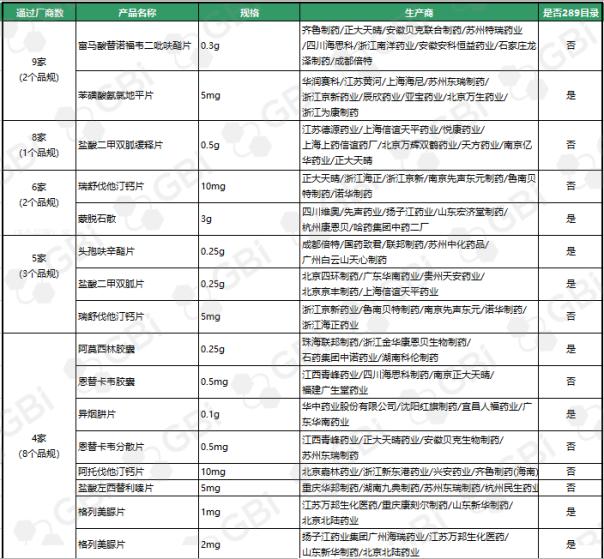
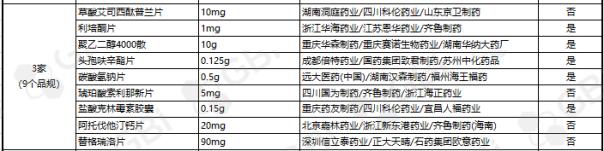
到现在,经过仿制药一致性点评或视同经过仿制药一致性点评经过企业达 3 家及以上品规共有25个。其间:
◆ 富马酸替诺福韦二吡呋酯片(0.3g)、苯磺酸氨氯地平片(5mg)有9家经过;
◆头孢呋辛酯片(0.25g)、盐酸二甲双胍片(0.25g)、瑞舒伐他汀钙片(5mg)有5家经过;
◆阿莫西林胶囊(0.25g)、恩替卡韦胶囊(0.5 mg)、异烟肼片(0.1g)、恩替卡韦分散片(0.5 mg)、阿托伐他汀钙片(10mg)、盐酸左西替利嗪片(5mg)、格列美脲片(1mg)、格列美脲片(2mg)8个品规现在已有4家企业经过仿制药一致性点评;
◆经过企业达 3 家的9个品规分别是:草酸艾司西酞普兰片(10mg)、利培酮片(1mg)、聚乙二醇4000散(10g)、头孢呋辛酯片(0.125g)、碳酸氢钠片(0.5g)、琥珀酸索利那新片(5mg)、盐酸克林霉素胶囊(0.15g)、阿托伐他汀钙片(20mg)、替格瑞洛片(90mg)。
据GBI SOURCE数据库显现,到2019年7月29日,CDE有关仿制药一致性点评累计受理号已达1324个,触及385家企业的302个种类,现在已有298个品规经过或视同经过仿制药一致性点评。其间:2个品规经过企业达9家;1个品规经过企业达8家;2个品规经过企业达6家;3个品规经过企业达5家;8个品规经过企业达4 家;9个品规经过企业达 3 家;24个品规经过企业达2家;138个品规经过企业达1家(具体名单见下表)。
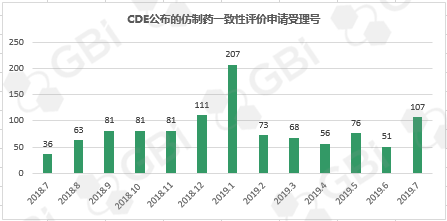
据GBI SOURCE数据库【药品申报状况计算】东西计算的成果为,2019年7月份CDE新受理了 107 个(数据计算到7月29日)仿制药一致性点评的请求,比较6月份增加近110%,这也是继2019年1月份后单月受理数初次打破三位数,猜测和7月中旬业界撒播出国家医保局关于药品 4+7 集采扩面的音讯不无关系。
乐普(北京)医疗器械股份有限公司部属公司参加广东联盟药品会集收购拟中标
更多
诺华没有ADC,但有7个核药管线亿美元,核药Pluvicto大增...
诺华没有ADC,但有7个核药管线亿美元,核药Pluvicto大增261%
2024年2月8日,Alector Therapeutics公司和GSK宣告,美国FDA已颁发在研抗...[具体]
光动力医治是一种由光照耀已进入人体安排细胞内的光敏剂而发生...[具体]
2024年2月5日,NMPA发布《国家药监局归纳司揭露寻求《中药规范管...[具体]
在医药范畴,如果说有令全员受损的行为,百健的阿尔茨海默病疗...[具体]
2月8日,南京征祥医药有限公司递送的「玛赛洛沙韦片」的上市申...[具体]
新闻中心
- 2025上海世界个护及日化美妆博览会2025-05-01
- 神驰机电 (603109)2025-05-01
- 【市占率认证】电机行业市占率分析有这些就够了!(智研咨询)2025-05-01
- 代表国内顶配水平!华能重庆两江燃机二期项目3号机组正式投运2025-05-01
- 方程豹钛3标配智驾 预售1398万起加24万就有四驱2025-05-01